HPV自采样操作方式和检测效果
本文来源于微信公众号圣检E讯
传统的宫颈癌筛查,进行HPV检测的样本都是在医院里由临床医生通过宫颈刷采样收集。常常面临着往返医院路途较远,预约麻烦或预约不上,在医院排队等候时间过长,面对医生的操作觉得尴尬等等问题,这些因素都使得HPV检测的筛查覆盖率并不高。因此,如何提高HPV检测的普及率,做到宫颈癌筛查“全覆盖”一直是研究的热点问题,HPV自采样技术就在这样的背景下顺势而生。
1、什么是HPV自采样?
“HPV自采样技术”顾名思义自采样就是指受检者无需前往医院等候医生取样,而是在家中自行完成宫颈脱落细胞取样的一种技术,再将样本寄到检测机构或者医院进行检测。
2、HPV自采样发展概况
2016年,荷兰的宫颈癌筛查方案从基于细胞学转为HPV筛查,发现HPV阳性者再进行细胞学检查,同时向女性发放HPV自采样器。
2017年,国际HPV大会(IFCPC)上决定在全球范围开展HPV自采样的研究和实践。
2017年,在CSCCP会议上,北京大学人民医院妇产科魏丽惠教授介绍了HPV自采样的全球共识,肯定了HPV自采样的效果。
2021年,世界卫生组织(WHO)发布了宫颈癌预防中宫颈癌前病变的筛查和治疗指南,建议优化诊断工具与筛查选择,推荐以人乳头瘤病毒(HPV)DNA检测作为宫颈癌筛查的首选筛查方法。至此,宫颈癌筛查正式从细胞学检查时代进入HPV DNA时代。
2023年,美国临床化学协会(American Association for Clinical Chemistry,AACC)总结了支持自行采集的阴道样本方法的文献,并表示这种方法可以改善人群的宫颈癌筛查[1]。
基于检测技术的高敏感性、高阴性预测值及客观性,HPV自采样被美国克利夫兰医学中心评为2017年度“影响人类未来的全球医学十大创新成果”之一[2]。
3、HPV自采样的效果如何?
在荷兰研究[3]中,8212名参与者被随机分配到自我采样组,8198名参与者被随机分配到临床医生采样组。在对HPV阳性女性的中位随访时间为20个月后,HPV检测的敏感性和特异性在自我采样和基于临床医生的采样之间在检测CIN2+或CIN3+病变方面没有差异。在墨西哥的研究中[4],12330名女性被随机分配到自行收集的阴道标本组并接受HPV基因分型,并对检测呈阳性的患者进行随访阴道镜检查。另有12731名患者被随机分配至仅接受宫颈细胞学检查,使用HPV检测自行采集的阴道标本识别CIN2或更严重的宫颈癌的相对敏感性比单独进行宫颈细胞学检查高3.4倍。日本的宫颈癌筛查率一直较低,他们同样进行了HPV自采样的研究[5],发现医生采样和自采样的总体阳性率分别为61.0%和40.4%,对于CIN2自采样的敏感性略低于医生采样(76.0% vs 59.4%),但是对于CIN3没有差异。
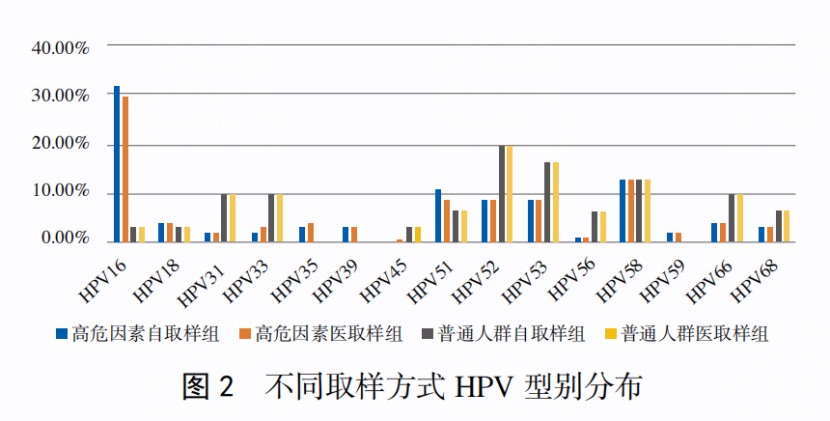
近日由北京大学人民医院魏丽惠教授和江西省妇幼保健院李隆玉教授等[6]团队发表的研究成果显示:使用圣湘生物HPV检测试剂发现,基于PCR 技术的HPV自取样检测在子宫颈癌筛查中的效果与医取样相似,且具有便捷、廉价、依从性高等优势,可用于子宫颈癌初筛,适合于普通人群和高危人群,有望为扩大子宫颈癌筛查覆盖率提供帮助。

普通人群女性以HPV52 阳性率最高,其次是HPV53、HPV58、HPV33和HPV31型,医取样和自取样分布一致;有高危因素女性中HPV 阳性率依次是 HPV16、HPV58、HPV51、HPV52和HPV53;医取样和自取样分布一致,见下图。
4、HPV自采样的可接受度如何?
2017年2月有研究报道[7]关于HPV自采样可接受度meta分析的文章,选择从1986年到2014年的37项研究,包括来自五大洲24个国家的18516名女性。报告显示女性对自我采样的接受程度高,最常见原因是易用性(91%),不尴尬(91%),保护隐私(88%),舒适感(88%),不用去医院(69%)和方便(65%)。当然也有人担心自采样会不准确,愿意有医生进行采样。大部分女性表示,她们更倾向于自采样与医生采样相结合的方式,在一定时间内进行自采样,届时再去医院进行医生采样。
5、HPV自采样的优势
(1) 提高宫颈癌筛查的接受度,提升了宫颈癌筛查的便捷性,使筛查人群覆盖面更广;
(2) 自采样减轻了患者的经济负担,节省了筛查成本,并使患者有了更强的隐私感和自主感;
(3) HPV自采样除可增加女性的可接受性和依从性外,还增加了常规筛选或从未筛选的患者与医师的接触机会,增加了随访率;
(4) HPV自采样可行性高,各种年龄段的女性均能通过简单的书面指导单独进行自采样测试;
(5) 方便女性定期筛查,使资源匮乏地区开展宫颈癌的普遍筛查成为可能。
6、HPV自采样怎样操作?
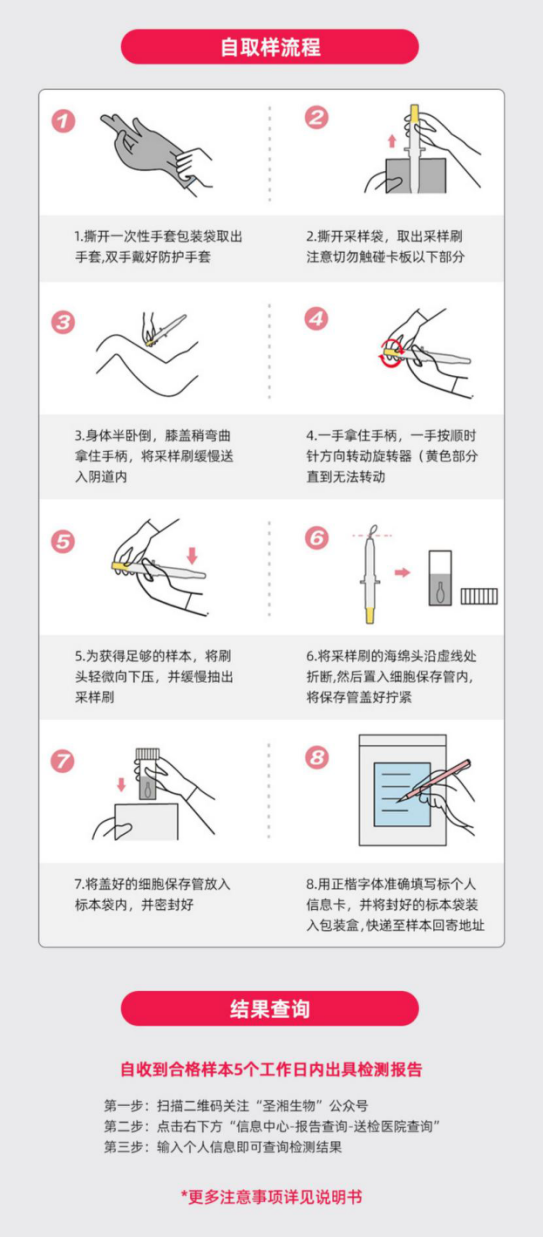
圣湘生物不仅有HPV自采样商品化服务,也可为各医疗机构提供HPV核酸检测试剂、仪器及HPV自采样耗材、信息化系统等配套的整体解决方案。 HPV自取样是一种很有前景的策略,可以克服资源匮乏地区宫颈癌筛查的多重障碍,并在筛查计划完善的国家增加筛查不足的女性的覆盖率。HPV自采样方法可能是提高宫颈癌筛查的可及性和采用率的唯一途径,尤其是在疾病负担最重的地区,并且现在被认为是实现WHO 消除宫颈癌这一目标的关键因素[8][9]。HPV自采样有非常明显的优势,使无需医务人员介入的大量初筛工作成为可能,降低筛查成本和提高筛查效率,使得“全覆盖”式的宫颈癌筛查成为可能,这种技术或许或将对宫颈癌的预防模式产生深远影响。
[参考文献]:
[1] Zhu Y, Feldman S, Leung SOA, Creer MH, Warrick J, Williams N, Mastoridese S. AACC guidance document on cervical cancer detection: screening, surveillance, and diagnosis. [Epub] J Appl Lab Med March 6, 2023, as doi: 10.1093/jalm/jfac142.
[2] 自取样HPV检测模式"获评"十大影响未来的全球医学创新成果[J].中华妇产科杂志,2017,52(5):353.
[3] Polman NJ, Ebisch RMF, Heideman DAM, et al. Performance of human papillomavirus testing on self-collected versus cliniciancollected samples for the detection of cervical intraepithelial neoplasia of grade 2 or worse: a randomised, paired screenpositive, non-inferiority trial[J]. Lancet Oncol 2019;20:229-38.
[4] Lazcano-Ponce E, Lorincz AT, Cruz-Valdez A, et al. Self-collection of vaginal specimens for human papillomavirus testing in cervical cancer prevention (MARCH): a community-based randomised controlled trial[J]. Lancet 2011;378:1868-73.
[5] Aiko KY1, Yoko M1, Saito OM, et al. Accuracy of self-collected human papillomavirus samples from Japanese women with abnormal cervical cytology[J]. J Obstet Gynaecol Res.2017,43(4):710-717.
[6] 涂开家,李静然,金强珍等. 不同人群自取样和医取样HPV检测用于子宫颈癌筛查分析. 中国妇产科临床杂志. 2023, 24(4): 408-410 https://doi.org/10.13390/j.issn.1672-1861.2023.04.018
[7] Nelson EJ, Maynard BR, Loux T, Fatla J, Gordon R, Arnold LD. The acceptability of self-sampled screening for HPV DNA: a systematic review and meta-analysis. Sex Transm Infect. 2017 ,93(1):56-61.
[8] WHO Guideline on self-care interventions for health and well-being. Available from: https://www.who.int/publications-detail-redirect/9789240030909 (2021).
[9] de Sanjose, F. Holme. What is needed now for successful scale-up of screening? Papillomavirus Res., 7 (2019 Apr 16), pp. 173-175.
注:图片源于网络 侵删
撰写 | 张赛
校稿 编审 | 缪为民 刘娟
编辑 | 谭易秋子